Содержание:
Система комплемента представляет собой многомолекулярную систему, состоящую из более чем 32 белков сыворотки, белков мембран клеток, рецепторов клеточных мембран, которые связываются с фрагментами комплемента. Белки системы комплемента составляют 10% содержания глобулинов сыворотки. Многие из этих белков обозначаются буквой C (C1, 4, 2, 3, 5, 6, 7, 8 и 9), им присвоены номера в порядке их открытия. Большинство из них синтезируется главным образом печенью. Исключениями являются C1, фактор (F) D и пропердин. Они, вероятно, синтезируются макрофагами и даже Т-лимфоцитами.
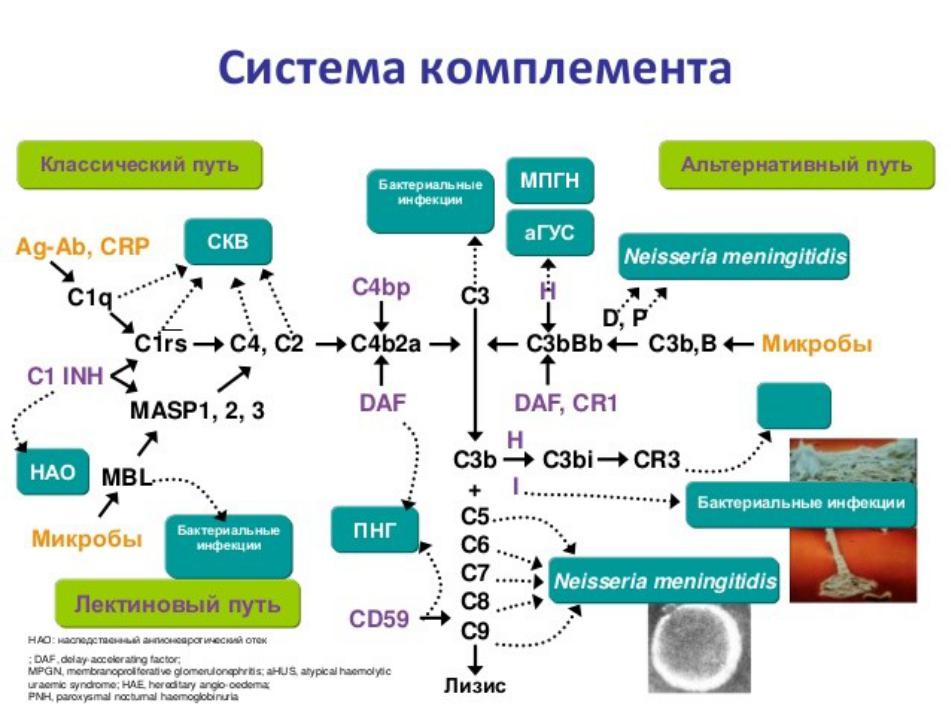
Активация системы комплемента
Белки системы комплемента циркулируют в плазме в неактивном состоянии. Активация инициируется широким спектром веществ и имеет 2 фазы. На первой фазе ряд специфических взаимодействий (три пути активации, рис.1) приводит к образованию собственной комплементарной протеиназы, называемой C3-конвертазой. Вторая фаза для каждого включает расщепление C3b, образование нескольких биологически важных фрагментов и больших, потенциально цитолитических комплексов.
Классический путь (КП)
Компоненты КП активации комплемента: С1, С2, С4
КП имеет 2 блока. Один блок распознавания состоит из тримолекулярного комплекса C1q, 2 молекул C1r и 2 молекул C1s, удерживаемых вместе кальцием. Другой блок активации C2, C3 и C4. Последовательность активации начинается со связывания 2 или более единиц распознавания C1q с Fc-антиген связывающей частью молекул IgG и IgM. Это вызывает конформационное изменение, приводящее к авто активации C1r, который затем расщепляет C1s в его активное состояние. Затем С1s действует аналогично С1-эстеразе и расщепляет С2 и С4 с образованием C2aC4b, который представляет собой С3-конвертазу, которая расщепляет С3 с образованием С3b. C1q также может быть активирован микоплазмами, РНК-вирусами, бактериальными эндотоксинами и клеточными мембранами некоторых органелл без присутствия антител.
Альтернативный путь (АП)
Компоненты активации комплемента по АП: B, D
АП активируется вирусами, грибами, бактериями, паразитами, ядом кобры, иммуноглобулином А и полисахаридами и образует важную часть защитного механизма, независимого от иммунного ответа. Здесь C3b связывается с F B, который расщепляется F D до Bb. Затем комплекс C3bBb действует как C3-конвертаза и генерирует больше C3b через петлю усиления. Связывание F H с C3b увеличивает его инактивацию F I. Пропердин стабилизирует его, предотвращая его инактивацию F H и I. АП не приводит к действительно неспецифической активации комплемента, потому что для А требуются конкретные типы соединений. Для инициации А он просто не требует специфических взаимодействий антиген-антитело.
Лектиновый путь (MBL)
Компоненты активации комплемента по MBL-пути: MBL, MAS P-1, MAS P-2, MAS P-3
Лектин или маннан-связывающий пути активируется подобно КП, за исключением того, что лектин заменяет антитело, а маннан-связывающие лектин-ассоциированные протеазы заменяют ферментативную активность C1. Вместо этого маннан-связывающий лектин связывается с остатками сахара на поверхности патогена. Маннан-связывающий лектин связан с сериновыми протеазами, подобными субкомпонентам C1r и C1s классического пути, которые также активируют C4 и C2, образуя классическую C3-конвертазу C4b2a.
Мембраноатакующий комплекс
Компоненты мембраноатакующего комплекса: С3, С5, С6, С7, С8, С9
Только 5 белков участвуют в прямом киллинге клеток. C2a4b3b из классического и MBL-путей или C3bBb из АП расщепляют C5. C5b связывается с C6, C7 и C8 с образованием макромолекулярных комплексов C5b-8, которые связываются с клеточными мембранами. Молекулы С9 связываются с встроенными в мембраны C5b-9, с образованием круглых поры, пронизывающих мембрану, и обусловливающих лизис клеток.
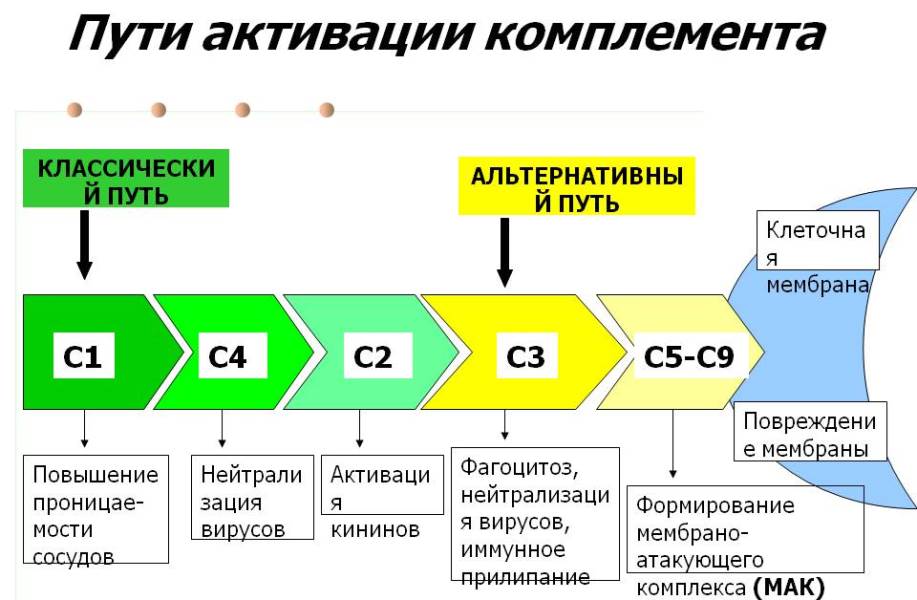
Регуляция путей активации комплемента
Белки регуляторы и рецепторы (Cl-ингибитор, C4-связывающий белок, F H, F I, пропердин, DAF, MCFP, CD59, CR1, CR2)
Система комплемента играет очень важную роль в защите хозяина, но если она направлена против хозяина, то может привести к серьезным заболеваниям. Поэтому практически каждый путь активации системы жестко контролируется (Рис.2).
Регуляция классического пути
Активация КП требует наличие антител на поверхности патогена (аутоантител на собственных клетках). C1-ингибитор (C1-INH) подавляет C1r и C1s путем ковалентного связывания с ними, вызывая распад макромолекулярного комплекса C1. Ингибитор синтезируется в печени и моноцитах крови; его ген расположен на хромосоме 11. Комплекс C2a4b очень лабилен и подвергается спонтанному распаду с высвобождением C2a и потерей ферментативной активности. С4-связывающий белок связывает С4, что ускоряет его диссоциацию с С2а и делает C4b более восприимчивым к протеолизу F I. F ускорения распада (DAF), связанный с мембранами способствует высвобождению C2a из C4b2a путем физического вмешательства в ассоциацию C4b и C2a.
Регуляция альтернативного пути
Углеводный состав на поверхности клеток и содержание в нем сиаловой кислоты играют важную роль в активации АП. Сиаловая кислота блокирует активацию, благоприятствуя связыванию F H с C3b, который затем инактивируется F I. Микроорганизмы, лишенные сиаловой кислоты, погибают, тогда как клетки человека, покрытые гликофорином А, сиалогликопротеином, защищены. C3bBb является относительно лабильным и подвергается спонтанному распаду посредством диссоциации Bb. Пропердин синтезируется моноцитами и Т-лимфоцитами. Пропердин связывается с C3bBb и стабилизирует его, предотвращая его распад. F H конкурирует с F B за связывание с C3b и вытесняет Bb из C3bBb. Он ускоряет инактивацию C3b F I. F I инактивирует C3b-iC3b, молекулу, которая не может функционировать как фермент. Рецептор комплемента 1 (CR1) обладает активностью, подобной F H, позволяющей F I расщеплять C3b. Мембранный кофакторный белок также обладает H-подобной активностью, главным образом для альтернативной конверсии C3.
Регуляция образования мембраноатакующего комплекса
Гомологический рестрикционный фактор, C8-связывающий белок, представляет собой белок клеточной мембраны со значительной гомологией последовательностей как с C8, так и с C9 и широко распространен в клетках периферической крови. Это предотвращает взаимодействие C8 и C9. Мембраносвязанный CD59, также известный как гомологичный рестрикционный фактор 20, предотвращает связывание C5b-8 с C9 и ингибирует п образование макроскопических пор в клеточной мембране. Протеин S (витронектин) связывается с C5b-7 и отменяет его активность. SP-40,40 (кластерин) оказывает эффекты, подобные витронектину.