Содержание:
Эозинофилы
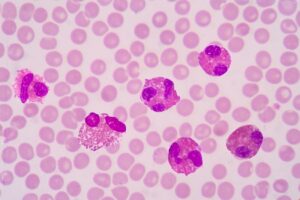 Эозинофилы (Э) представляют собой гранулоциты, способные окрашиваться кислым красителем эозином. Эозинофилия крови и тканей является признаком в инфекции гельминтами, аллергии, астмы, эозинофильных желудочно-кишечных расстройств, а также ряда других редких заболеваний.
Эозинофилы (Э) представляют собой гранулоциты, способные окрашиваться кислым красителем эозином. Эозинофилия крови и тканей является признаком в инфекции гельминтами, аллергии, астмы, эозинофильных желудочно-кишечных расстройств, а также ряда других редких заболеваний.
Морфология и фенотип
Э человека имеют двулопастное ядро с сильно конденсированным хроматином и два основных типа гранул, специфические и первичные. Специфические гранулы имеют характерный ультраструктурный вид с электронно-плотным кристаллоидным ядром и содержат катионные белки, которые определяют у Э уникальные свойства при окрашивании. Основными катионными белками в специфических гранулах являются главный основной белок (MBP), эозинофильная пероксидаза (EPO), эозинофильный катионный белок (ECP) и эозинофильный нейротоксин (EDN). Первичные гранулы аналогичны тем, которые встречаются в других линиях гранулоцитов, образуются на ранних стадиях развития Э и обогащены кристаллическим белком Шарко-Лейдена. Эозинофилы также содержат липидные тела, которые представляют собой цитоплазматические структуры, лишенные окружающей мембраны, содержат ферменты синтеза эйкозаноидов и являются основным местом синтеза.эйкозаноидов.
Э выражают массив молекул клеточной поверхности (Рис), включая рецепторы иммуноглобулина для IgG (FcγRII / CD32) и IgA (FcαRI / CD89); рецепторы комплемента (CR1 / CD35, CR3 и CD88); рецепторы цитокинов (IL-3R, IL-5R, GM-CSF, которые способствуют развитию Э, а также рецепторы IL-1, IL-2, IL-4, IFN- и TNF-α); хемокины (CCR1 и CCR3); молекулы адгезии (очень поздний антиген 4 (VLA4) α4β7) и SIGLES8; лейкотриеновые рецепторы (CysLT1R и CysLT2R; рецептор LTB4); рецепторы простагландинов (рецептор типа 2 PGD2); рецептор фактора активации тромбоцитов (PAF); и toll-подобные рецепторы (в частности, TLR7 / 8). Экспрессия FcεRRI на эозинофилах минимальна, не активирует эозинофилы и не имеет четкого функционального значения.
Развитие и локализация у человека
 IL-5, IL-3 и GM-CSF способствуют развитию Э из CD34+ гемопоэтических клеток-предшественников, хотя только для IL-5 характерна специфичность влияния на развитие и дифференцировку Э. Плюрипотентные гемопоэтические стволовые клетки вначале дифференцируются в предшественник эозинофилы / базофилы, затем следует линия Э. Направленность дифференцировки определяет экспрессия CD34, IL-5R и CCR3. Э созревают в костном мозге и высвобождаются в кровообращение после стимуляции IL-5, Большой пул зрелых Э остаются в костном мозге. IL-5, продуцируемый в местах аллергического воспаления или инфекции гельминтами, действует дистально на костный мозг и инициирует выход Э в кровоток и соответствующие ткани.
IL-5, IL-3 и GM-CSF способствуют развитию Э из CD34+ гемопоэтических клеток-предшественников, хотя только для IL-5 характерна специфичность влияния на развитие и дифференцировку Э. Плюрипотентные гемопоэтические стволовые клетки вначале дифференцируются в предшественник эозинофилы / базофилы, затем следует линия Э. Направленность дифференцировки определяет экспрессия CD34, IL-5R и CCR3. Э созревают в костном мозге и высвобождаются в кровообращение после стимуляции IL-5, Большой пул зрелых Э остаются в костном мозге. IL-5, продуцируемый в местах аллергического воспаления или инфекции гельминтами, действует дистально на костный мозг и инициирует выход Э в кровоток и соответствующие ткани.
Период полувыведения Э в из кровообращении составляет 8-18 часов. Подавляющее большинство Э расположены в тканях, особенно на поверхностях слизистой оболочки желудочно-кишечного тракта и в очагах воспаления с преобладанием Th2. IL-4 и IL-13 играют центральную роль в заселении Э слизистой оболочки путем усиления активности эотаксина (CCL11 и CCL26) и экспрессии молекул адгезии на эндотелиальных клетках (VCAM-1). В отличие от эотаксинов, IL-5 не играет ключевой роли в продвижении проникновения Э в ткани. Фактор активации тромбоцитов (PAF), LTD2, C5a и CCL5 (RANTES) также являются мощными хемотаксическими факторами Э. Выживанию эозинофилов в тканях способствуют ИЛ-3, ИЛ-5.
Активация
Консенсуса в отношении основного механизма сигнализации для активации Э нет. Э могут быть активированы путем сшивания рецепторов IgG или IgA Fc агарозными гранулами с IgG, IgA или секреторным IgA, причем последний является наиболее эффективным. Э могут быть праймированы несколькими медиаторами, включая IL-3, IL-5, GM-CSF, CC-хемокины и фактор активации тромбоцитов. Результат активации варьирует. Сообщалось о четырех механизмах дегрануляции эозинофилов: экзоцитоз, сложный экзоцитоз, последовательный экзоцитоз и цитолиз. Различные медиаторы активации могут дифференцированно влиять на тип дегрануляции и факторы, освобождаемые Э в активированном состоянии. Детали этого процесса остаются неизвестными.
Медиаторы и эффекторные функции
Эозинофилы освобождают провоспалительные медиаторы, включая катионные белки, содержащие гранулы, вновь синтезированные эйкозаноиды и цитокины (рис.1). Главный основной белок (MBP) составляет более 50% массы белка гранул Э и является основным компонентом кристаллоидных ядер специфических гранул. MBP имеет большой положительный заряд, не обладает ферментативной активностью; считается, что токсичность белка опосредуется повышенной проницаемостью мембраны, возникающей в результате взаимодействия катионного белка с плазматической мембраной. MBP обладает активностью in vitro против паразитов, включая гельминты и шистосомы. У пациентов с астмой содержание MBP в сыворотке и бронхоальвеолярной лаважной жидкости прямо коррелируют с гиперреактивностью бронхов.
Эозинофильный нейротоксин (EDN) и эозинофильный катионный белок (ECP), оба имеют активность РНКазы, локализуются в матрице специфических гранул и проявляют токсичность in vitro к паразитам и одноцепочечным РНК пневмовирусам, включая респираторно-синцитиальный вирус. Хотя оба белка обладают активностью РНКазы тем не менее, активность EDNECP. Эозинофильная пероксидаза (ЕРО) представляет собой высоко катионный белок, локализованный в матрице специфических гранул и составляющий ~ 25% белка гранулы.
EPO катализирует окисление галогенидов, псевдогалогенидов и оксида азота до продуктов окисления, которые являются токсичными для микроорганизмов и клеток-хозяев.
Кристаллический белок Шарко-Лейдена (галектин -10) представляет собой гидрофобный белок неизвестной функции, который вырабатывается в большом количестве в эозинофилах. Белок хранится в первичных гранулах и высвобождается с активацией эозинофила. Кристаллы этого белка могут быть обнаружены в стуле или мокроте пациентов с желудочно-кишечной или респираторной эозинофилией.
Эозинофилы также являются источником липидных медиаторов, включая LTC4, PGE2, тромбоксан и фактор активации тромбоцитов. Хотя белки гранул являются основными эффекторными молекулами эозинофилов, эозинофилы способны продуцировать ряд цитокинов и хемокинов, включая TGF-β, IL-3, IL-4, IL-5, IL-8, IL-10, IL-12, IL-13, IL-16, IL-18, TNF-α, CCL5 и CCL11. Эозинофильные цитокины хранятся в гранулах, и быстро освобождаются при дегрануляции. Однако эозинофилы обычно продуцируют меньшее количество цитокинов, чем другие лейкоциты, и нет данных о существенной роли секреции цитокинов эозинофилами при защите от болезней. Эозинофилы демонстрируют иммуномодулирующую активность посредством множественных механизмов, включая секрецию цитокинов, представления антигена или экспрессии индоламина 2,3-диоксигеназы.
Роль в здоровье и болезни
Абсолютное содержание Э в периферической крови в норме до 500 / мм3 является нормальными и имеют суточные вариации, с самыми низкими уровнями по утрам и самым высоким уровнем в вечернее время. Повышение Э в периферической крови и тканях типично для ряда заболеваний, таких как аллергические заболевания, включая атопическую астму (обычно легкая эозинофилия), лекарственные реакции, гельминтозы и гиперэозинофильные синдромы. Эозинофилия также может быть отмечена при специфических первичных иммунодефицитных заболеваниях, прежде всего синдроме Оменна и гипер-IgE-синдроме. Эозинопения обычно наблюдается при острых бактериальных или вирусных инфекциях и при системном лечении кортикостероидами. Наличие эозинофилии у температурящего пациента должно вызвать подозрение на возможную недостаточность надпочечников.
Аллергические заболевания, включая аллергический ринит, атопическую астму и атопический дерматит, могут быть связаны с легкой эозинофилией периферической крови, хотя тканевые Э и Э в носовых выделениях, мокроте и лаважной жидкости могут быть значительно увеличены. Лечение анти-IL-5 у различных астматиков продемонстрировало 90% снижение количества Э в крови, но только 50% снижение Э в тканях и минимальное улучшение симптомов астмы. В настоящее время существует большая оценка того, что существует множественные фенотипы астмы, включая фенотипы на основе воспалительных механизмов (например, эозинофильные, нейтрофильные. Лечение пациентов анти-ИЛ-5, с «эозинофильной астмой», резистентных к лечению кортикостероидами, продемонстрировали значительное улучшение показателей Э периферической крови и мокроте и улучшение симптомов астмы.
Гиперэозинофильные синдромы (ГЭС) представляют собой гетерогенную группу расстройств, характеризующуюся: выраженным увеличением эозинофилов в периферической крови (> 1500 / мм3); стойкой эозинофилией и / или свидетельством повреждения определенного органа; при исключении известных причин эозинофилии, включая паразитарные инфекции и лекарственные реакции. Эти заболевания были разделены на 6 групп: 1) миелопролиферативный вариант -эозинофильный лейкоз; 2) лимфоцитарный вариант (клональное увеличение Т-клеток, секретирующих IL-5), 3) семейный (семейный анамнез стойкой эозинофилии без идентифицируемой причины), 4) неопределенный (включает доброкачественную эозинофилию без участия конечного органа и эозинофилии, связанной с рецидивным ангионевротическим отеком 5) гиперэозинофилия с ограниченными эозинофильными нарушениями органов — эозинофильные желудочно-кишечные расстройства или эозинофильная пневмония и 6) гиперэозинофилия, связанная с синдромом Чарга-Стросса, мастоцитозом, Лечение этих расстройств начато раньше, чтобы предотвратить повреждение конечных органов. Системные кортикостероиды — это лечение первой линии для большинства форм ГЭС. Дополнительно варианты ГЭС реагируют на иматиниб и меполизумаб.
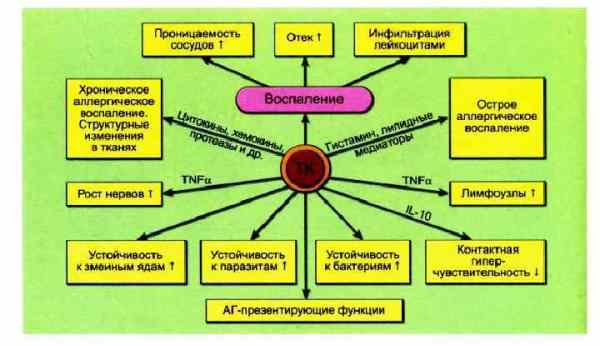
Тучные клетки, базофилы и эозинофилы экспрессируют много одних и тех же рецепторов и цитокинов, но имеют различные эффекторные функции. Тучные клетки являются тканевыми резидентными клетками и уникально необходимы для немедленной гиперчувствительности. Базофилы являются в основном циркулирующими клетками, но являются основой аллергического воспаления во время поздней фазы ответа.
Эозинофилы являются жителями ЖКТ, но основой локальных аллергических воспалений.
Доминирующие цитокины, продуцируемые этими клетками, различаются: базофилы обильно секретируют IL-4 и IL-13, но немного IL-5, тогда как тучные клетки продуцируют IL-5 и IL-13, но немного IL-4. Хотя эозинофилы могут экспрессировать ряд цитокинов, их главной эффекторной функцией считают катионные белки специфических гранул. Различия в расселении, активации и синтезе медиаторов вносят вклад в уникальную роль ТК, Б и Э.