Содержание:
Определение
 Нейтропения — состояние, при котором число циркулирующих нейтрофилов меньше 1500/мкл. Независимо от причины, клиническое проявление нейтропении – повышенная восприимчивость к бактериальным инфекциям, с частотой и тяжестью прямо пропорциональными степени нейтропении. Выделяют мягкую нейтропению, когда количество нейтрофилов лежит в пределах 1000 – 1500/мкл, умеренную, когда нейтрофилы составляют 500 – 1000/мкл и тяжелую, когда количество нейтрофилов меньше 500/мкл. Другие факторы, которые могут влиять на тяжесть инфекционного диатеза у пациента с нейтропенией:
Нейтропения — состояние, при котором число циркулирующих нейтрофилов меньше 1500/мкл. Независимо от причины, клиническое проявление нейтропении – повышенная восприимчивость к бактериальным инфекциям, с частотой и тяжестью прямо пропорциональными степени нейтропении. Выделяют мягкую нейтропению, когда количество нейтрофилов лежит в пределах 1000 – 1500/мкл, умеренную, когда нейтрофилы составляют 500 – 1000/мкл и тяжелую, когда количество нейтрофилов меньше 500/мкл. Другие факторы, которые могут влиять на тяжесть инфекционного диатеза у пациента с нейтропенией:
- скорость развития и продолжительность нейтропении,
- миелоидный резерв костного мозга,
- абсолютное число циркулирующих моноцитов,
- функциональное состояние фагоцитов.
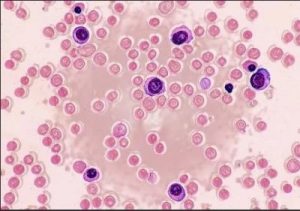 Тяжелая врожденная нейтропения (болезнь Костмана) относится к группе редких врожденных иммунодефицитов. Тяжелая врожденная нейтропения характеризуется низким уровнем или полным отсутствием нейтрофильных гранулоцитов (агранулоцитоз). Нейтрофильные гранулоциты — это белые клетки крови, лейкоциты, которые являются частью нормальной иммунной системы и обычно преобладают среди других групп лейкоцитов. Одно из свойств нейтрофильных гранулоцитов — способность к фагоцитозу. Эти клетки быстро и эффективно перемещаться из крови к источникам инфекции и поглощают инородные частицы, в том числе бактерии.
Тяжелая врожденная нейтропения (болезнь Костмана) относится к группе редких врожденных иммунодефицитов. Тяжелая врожденная нейтропения характеризуется низким уровнем или полным отсутствием нейтрофильных гранулоцитов (агранулоцитоз). Нейтрофильные гранулоциты — это белые клетки крови, лейкоциты, которые являются частью нормальной иммунной системы и обычно преобладают среди других групп лейкоцитов. Одно из свойств нейтрофильных гранулоцитов — способность к фагоцитозу. Эти клетки быстро и эффективно перемещаться из крови к источникам инфекции и поглощают инородные частицы, в том числе бактерии.
Нейтрофильные гранулоциты образуются в костном мозге и со скоростью 1,1х106 клеток в секунду поступают в кровь, где циркулируют в ожидании сигнала из тканей 5-7 часов. Если из ткани не поступил сигнал тревоги — не было бактериального или грибкового инфицирования, то нейтрофилы крови подвергаются запрограммированной смерти, апоптозу, рассыпаются на мелкие пузырьки, их место занимают нейтрофилы свежей генерации.
Симптомы
 Дефицит нейтрофильных гранулоцитов при тяжелой врожденной нейтропении приводит к серьезным бактериальным инфекциям. Первые симптомы болезни часто проявляются уже при рождении или в течение первых недель жизни. Большинство инфекций при тяжелой врожденной нейтропении вызваны бактериями на коже или на слизистых оболочках. У детей с тяжелой врожденной нейтропенией часто развиваются фурункулы, инфекции пуповины и тяжелые инфекции полости рта. При тяжелой врожденной нейтропении периодическое воспаление среднего уха является обычным явлением, как и серьезные инфекции, включая пневмонию и сепсис. Если эти состояния не лечить антибиотиками, они могут привести к опасным для жизни инфекциям.
Дефицит нейтрофильных гранулоцитов при тяжелой врожденной нейтропении приводит к серьезным бактериальным инфекциям. Первые симптомы болезни часто проявляются уже при рождении или в течение первых недель жизни. Большинство инфекций при тяжелой врожденной нейтропении вызваны бактериями на коже или на слизистых оболочках. У детей с тяжелой врожденной нейтропенией часто развиваются фурункулы, инфекции пуповины и тяжелые инфекции полости рта. При тяжелой врожденной нейтропении периодическое воспаление среднего уха является обычным явлением, как и серьезные инфекции, включая пневмонию и сепсис. Если эти состояния не лечить антибиотиками, они могут привести к опасным для жизни инфекциям.
У новорожденных при тяжелой врожденной нейтропении или нарушении функции нейтрофилов необычно долго не отпадает пупочная культя. Поэтому, если у новорожденных пупочная культя не отпадает в течение 6 недель, необходимо определить в его крови абсолютное содержание нейтрофилов и оценить их функцию.
У детей с тяжелой врожденной нейтропенией до прорезывания первых зубов часто появляются болезненные язвы слизистой полости рта. После прорезывания зубов развивается воспаление десен (гингивит), часто хронический, который может привести к потере зубов у детей дошкольного возраста. Хроническое воспаление при тяжелой врожденной нейтропении сопровождается кровоточивостью десен при чистке зубов.
Периодические инфекции влияют на общее состояние здоровья детей и они отстают в росте. Рост остается ограниченным даже после курса лечения.
Тяжелая врожденная нейтропения является одним из синдромов группы заболеваний, вызываемых врожденной недостаточностью костного мозга. Многие из этих заболеваний являются факторами повышенного риска развития миелодисплазии и острого миелоидного лейкоза. Миелодиспластический синдром связан с серьезными нарушениями функции костного мозга и образования клеток крови. Последнее приводит к дефициту различных видов клеток крови и обычно трансформируется в острый миелоидный лейкоз. У лиц с приобретенными хроническими нейтропениями риск развития миелодиспластического синдрома и острого миелоидного лейкоза отсутствует.
Диагностика
Анализ крови при бактериальных инфекциях включает определение числа лейкоцитов, лейкограмму, определение абсолютного содержания нейтрофилов, содержание гемоглобина и тромбоцитов, содержание IgG. Тяжелую врожденную нейтропению можно заподозрить, если количество нейтрофильных гранулоцитов ниже 500 / мкл. Заболевание связано с довольно низким уровнем гемоглобина крови, повышенным уровнем тромбоцитов, а также увеличением числа моноцитов (другой тип лейкоцитов). Часто повышен уровень IgG. Большинство из этих изменений результат хронического воспаления.
Если подозревается болезнь Костманна, должен исследоваться костный мозг. При тяжелой врожденной нейтропении блокируется созревание нейтрофилов из клеток предшественников.
 Диагноз может быть подтвержден анализом ДНК — установление мутации в Elane, HAX1 или некоторых других известных генах.
Диагноз может быть подтвержден анализом ДНК — установление мутации в Elane, HAX1 или некоторых других известных генах.
Хромосомный анализ клеток костного мозга следует проводить, когда диагноз тяжелой врожденной нейтропении установлен, и пациенту выполняются регулярные медицинские осмотры. Хромосомные аномалии могут быть предвестником лейкемии. Ежегодно в клетках костного мозга следует исследовать ген рецептора колониестимулирующего фактора гранулоцитов (G-CSF); мутации в этом гене могут быть признаком начала лейкемии.
Независимо от типа мутации, которая вызывает тяжелую врожденную нейтропению, при неясном диагнозе или на ранней стадии заболевания целесообразно определить содержание в крови белка LL-37, низкие уровни этого белка патогномоничны для тяжелой врожденной нейтропении.