Содержание:
Иммунная система
 Каждый живой организм, в том числе наш собственный, должен постоянно быть настороже, чтобы его не сожрали другие, поскольку он представляет собой потенциальный источник ценных органических молекул. Способность противостоять использованию в качестве «пищи» автоматически дает избирательное преимущество. В ходе эволюции это привело к созданию высокотехнологичных систем защиты в многоклеточных организмах.
Каждый живой организм, в том числе наш собственный, должен постоянно быть настороже, чтобы его не сожрали другие, поскольку он представляет собой потенциальный источник ценных органических молекул. Способность противостоять использованию в качестве «пищи» автоматически дает избирательное преимущество. В ходе эволюции это привело к созданию высокотехнологичных систем защиты в многоклеточных организмах.
Чтобы сохранить целостность нашего организма, важно различать биологические структуры, с которыми нужно бороться, все, что представляют опасность для нашего организма, и структуры, на которые нельзя нападать, например, клетки нашего собственного тела или полезные бактерии в нашем кишечнике. Эта проблема вовсе не тривиальна, так как опасные нападающие из миров вирусов, бактерий и паразитов состоят в основном из тех же молекул, что и человеческий организм.
В начале эволюции простые многоклеточные организмы разработали защитную систему (ЗС), активируемую путем определения типичных молекулярных структур, связанных с патогенами или поврежденными клетками. Эта ЗС сохраняется и также работает у людей. Это врожденная, с готовыми блоками, работающая по принципу «один размер для всех» иммунная система, доступна тотчас. В лучшем случае она в корне пресекает начальную инфекцию; в худшем случае — держит инфекцию в течение нескольких дней под контролем. Мы все абсолютно зависим от этой «старой» ЗС: инфекционные агенты распространяются так быстро, что мы были бы мертвы задолго до того, как вторая, эволюционно более молодая иммунная система имела шанс нанести удар.
Наши наиболее эффективные защитные механизмы организуют специальную контратаку против конкретного инфекционного агента, вторгающегося в наш организм. Мы называем это адаптивным иммунным ответом. Работа на заказ требует времени, то есть ЗС просто не готова к использованию в первые дни заражения. Эти иммунные механизмы борются с «чужим» органическим материалом, который вошел в наше тело. «Чужой» не обязательно эквивалентен «опасный», но легче отличить «чужое» от «своего», чем отличать «опасное» от «безобидного». Это потому, что наша иммунная система способна узнать, что является «своим»; все остальное рассматривается с подозрением. В качестве дополнительных критериев для оценки уровня опасности учитывается активация первой, врожденной ЗС.
Врожденный иммунитет
 Несколько систем белков плазмы и клеточных систем вносят вклад во врожденный, неадаптивный иммунитет:
Несколько систем белков плазмы и клеточных систем вносят вклад во врожденный, неадаптивный иммунитет:
Плазменные белковые системы:
- система комплемента,
- система свертывания и фибринолитическая система,
- кининовая система.
Клеточные системы:
- полиморфноядерные гранулоциты (ПЯЛ),
- тучные клетки,
- эндотелиальные клетки,
- тромбоциты (тромбоциты),
- макрофаги,
- дендритные клетки,
- NK (естественные киллеры) и другие врожденные лимфоидные клетки.
Некоторые из этих типов клеток вносят вклад в молекулярные системы, которые необходимы для выполнения их защитных функций. В совокупности продукты секреции иммунокомпетентных клеток называют «медиаторы воспаления». Они либо предварительно сформированы, либо вновь синтезируются при потребности. Хотя эти молекулы на самом деле вызывают воспаление, их конечной целью является, конечно, не воспаление, а защита. Воспаление является переходным состоянием, которое облегчает борьбу с инфекционными агентами. Все эти молекулы сильно перекрываются в своих функциях. Эволюционное давление, по-видимому, благоприятствовало тому организму, у которого были резервные системы.
Недостаток: если мы хотим подавить нежелательное воспаление, мы, как правило, можем его только смягчить, но не полностью его подавить.
Медиаторы воспаления
Предварительно сформированные молекулы хранятся в гранулах и высвобождаются при необходимости:
- вазоактивные амины: гистамин, серотонин,
- лизосомальные белки.
Вновь синтезированные молекулы:
- простагландины и лейкотриены,
- фактор активации тромбоцитов (ФАТ),
- активные формы кислорода (АФК),
- NO,
- цитокины,
- интерфероны типа I.
КОМПЛЕМЕНТ
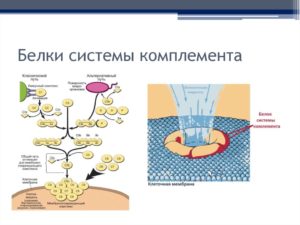
Система комплемента (СК) — это более чем 30 белков плазмы крови, которые называют компонентами или факторами. В основном служит для борьбы с бактериальными инфекциями. Она работает на нескольких уровнях. СК имеет базовую функцию распознавания многих бактерий, может праймировать и привлекать фагоциты, улучшать распознавание бактерий фагоцитами, а иногда даже лизировать бактерии.
Система комплемента может быть активирована по меньшей мере тремя отдельными путями. Два эволюционно более старых пути — это так называемые «альтернативный» и лектиновый пути. Оба активируются на многих бактериальных поверхностях, что способствует врожденному иммунитету. Третий путь, который в основном активируется антителами и, следовательно, является частью адаптивной иммунной системы, развился значительно позже, но был идентифицирован первым. Несколько несправедливо, поэтому его называют «классическим путем».
Альтернативный путь активации комплемента начинается со спонтанного гидролиза внутренней тиоэфирной связи плазменного компонента комплемента C3, по месту разрыва связи присоединяется вода, в результате чего получается C3 (H2O). Измененная конформация С3(Н2О) позволяет связывать белковый фактор B плазмы, который, в свою очередь, расщепляется на фрагменты Ba и Bb с помощью протеазы плазмы фактора D. Хотя Bb способен к диффузии, комплекс C3(H2O)Bb представляет собой растворимую C3-конвертазу, которая расщепляет ряда молекул С3, что приводит к образованию небольшого растворимого С3а и большего фрагмента С3b, который обычно быстро инактивируется. В случае, когда С3b образуется вблизи поверхности бактерий или клеток, он ковалентно связывается с этой поверхностью. Только что описанный процесс повторяется на мембране: фактор B прикрепляется и расщепляется фактором D. Дальнейшее развитие зависит от природы рассматриваемой поверхности. Если C3b связывается с мембраной одной из наших собственных клеток, процесс активации ингибируется одним из нескольких различных защитных белков, предотвращая повреждение клетки. На бактериальной поверхности эти ингибиторы отсутствуют, что позволяет продолжить каскад комплемента. Захваченный бактериальной поверхностью, фактор P (пропердин) стабилизирует связанный с мембраной комплекс C3bBb. Этот комплекс, C3-конвертаза альтернативного пути, впоследствии работает как инструмент усиления, быстро расщепляя сотни дополнительных молекул C3. Растворимый C3a диффундирует в окружающую среду, мобилизуя путем хемотаксиса фагоциты к месту инфекции. С3b-фрагменты и их продукты расщепления C3d, C3dg и C3bi включаются в бактериальную поверхность в возрастающем количестве и распознаются специфическими рецепторами комплемента (CR1-CR4), присутствующими на мембране фагоцитов. Эта функция превращения бактерий в «деликатес» для фагоцитов, называется опсонизацией, от греческого слова «goody». Каскад комплемента не останавливается на этом этапе: дальнейшая активация компонентов С5-С9 в конечном итоге приводит к образованию пор в мембране, которым иногда удается лизировать бактерии.
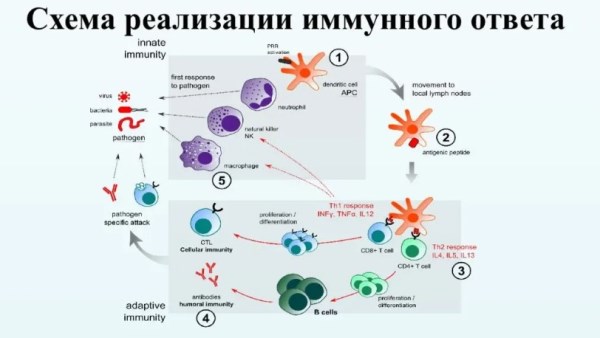
Меньшие продукты расщепления C3a, C4a, C5a, иногда называемые «анафилатоксинами», имеют дополнительные функции сами по себе: помимо привлечения фагоцитов они вызывают дегрануляцию тучных клеток и повышают проницаемость сосудов, тем самым облегчая доступ к месту внедрения инфекции белков плазмы и лейкоцитов.
Лектиновый путь активации комплемента. В плазме крови циркулирует комплекс олигомерного белка маннансвязывающего лектина (MBL) и двух сериновых протеаз MASP-1 и MASP-2. Многие бактериальные поверхности содержат в составе углеводов молекулы сахара маннозы. MBL связывается с маннозой, при этом протеазы MASP-1 и MASP-2 активируются. Они, расщепляя C4 и C2, генерируют второй тип C3-конвертазы, состоящей из C4b и C2b, с последующими реакциями, идентичными событиям альтернативного пути.
Классический путь обычно инициируется связанными с бактериами антителами IgG (две молекулы) и IgM, захватывающих компонент C1q, с последующим связыванием и последовательной активацией сериновых протеаз C1r и C1s. C1s расщепляет C4 и C2, причем C4b и C2b образуют C3-конвертазу классического пути. Тем не менее этот путь можно также активировать в отсутствие антител C-реактивным белком плазмы, который связывается с бактериальными поверхностями и способен активировать C1q.
*NB: гуманизированное моноклональное антитело Eculizumab связывается с компонентом комплемента C5, ингибируя его расщепление и предотвращая активацию литического пути. Это полезно, когда активация комплемента вызывает нежелательный гемолиз, как при пароксизмальной ночной гемоглобинурии или при некоторых формах гемолитического уремического синдрома. При менингококковых инфекциях лечение Eculizumab увеличивает риск этих инфекций, что может быть предотвращено предварительной вакцинацией.
Место и роль только C3a в организации иммунного ответа отражает рис. 2.
Система свертывания крови/фибринолиза и кининовая система
 Часто свертывание крови и кининовая системы активируются одновременно процессом, называемым контактной активацией. Как следует из названия, этот процесс инициируется, когда образуется комплекс из трех белков плазмы при контакте с некоторыми отрицательно заряженными поверхностями. Такими поверхностями могут быть коллаген, базальные мембраны или агрегированные тромбоциты в случае раны или бактериальные поверхности в случае инфекции.
Часто свертывание крови и кининовая системы активируются одновременно процессом, называемым контактной активацией. Как следует из названия, этот процесс инициируется, когда образуется комплекс из трех белков плазмы при контакте с некоторыми отрицательно заряженными поверхностями. Такими поверхностями могут быть коллаген, базальные мембраны или агрегированные тромбоциты в случае раны или бактериальные поверхности в случае инфекции.
Три рассматриваемых плазменных белка — фактор Хагемана (фактор свертывания XII), высокомолекулярный кининоген (ВМК) и прекалликреин. Фактор XII активируется при контакте с отрицательно заряженной поверхностью, начиная весь каскад коагуляции. Кроме того, фактор XII расщепляет прекалликреин, высвобождая активную протеазу калликреин, которая, в свою очередь, высвобождает нонапептидный брадикинин из высокомолекулярного кининогена (ВМК). Брадикинин усиливает проницаемость мелких сосудов, косвенно через эндотелий расширяет небольшие сосуды, но в остальном способствует сокращению гладких мышц и является самым сильным медиатором боли. Брадикинин и другие кинины имеют короткий период полувыведения, инактивируются пептидазами, включая ангиотензин превращающий фермент (АПФ).
NB: ингибиторы АПФ, часто используемые для снижения артериального давления, имеют общий побочный эффект- кашель. Считается, что это связано с увеличением активности брадикинина.
Результатом каскада активации плазменных белков является началом воспалительной реакции и блокирование небольших венул путем свертывания, что полезно для предотвращения распространения инфекции через кровь. Под действием артериального давления плазма фильтруется из сосудов с повышенной проницаемостью, образуя тканевую лимфу. Лимфа фильтруется через региональные лимфатические узлы, где фагоциты и другие лейкоциты ждут, чтобы включиться в защиту.
Каскад активация плазменных белков во многих отношениях является предварительным условием для следующего этапа, активации клеточных систем на месте заражения. Как активируются участвующие клетки?