Содержание:
Что это такое?
 Врожденный иммунитет — это первая линия обороны иммунной системы, которая включает предсуществующие механизмы защиты, всегда готовые к быстрой, стереотипной обороне. Рецепторы клеток врождённого иммунитета генетически закодированы и неизменны в течение жизни; на поверхности микроорганизмов они распознают структуры жизненно важных для микробов молекул, которые не могут быть изменены в результате одной мутации. Клетки врожденного иммунитета одного и того же типа имеют одинаковый набор рецепторов. Они находят и убивают болезнетворные микроорганизмы и одновременно активируют адаптивный иммунный ответ. Врожденный (неспецифический) иммунитет обеспечивает защиту с умеренной эффективностью в течение нескольких дней, пока не активируется адаптивный иммунитет. Адаптивный иммунитет для активации требует от нескольких дней до недели. Адаптивный иммунитет специфический, его составляющие научены ответу на точные молекулярные структуры. Для создания своих рецепторов адаптивный иммунитет использует перегруппировку генов (реаранжировку), и пролиферацию клеток со специфическими рецепторами путем формирования клонов. Адаптивный иммунитет имеет иммунологическую память. Адаптивная иммунная система — дополнение к эволюционно более древней врождённой иммунной системе, обеспечивающее специфичность распознавания и память.
Врожденный иммунитет — это первая линия обороны иммунной системы, которая включает предсуществующие механизмы защиты, всегда готовые к быстрой, стереотипной обороне. Рецепторы клеток врождённого иммунитета генетически закодированы и неизменны в течение жизни; на поверхности микроорганизмов они распознают структуры жизненно важных для микробов молекул, которые не могут быть изменены в результате одной мутации. Клетки врожденного иммунитета одного и того же типа имеют одинаковый набор рецепторов. Они находят и убивают болезнетворные микроорганизмы и одновременно активируют адаптивный иммунный ответ. Врожденный (неспецифический) иммунитет обеспечивает защиту с умеренной эффективностью в течение нескольких дней, пока не активируется адаптивный иммунитет. Адаптивный иммунитет для активации требует от нескольких дней до недели. Адаптивный иммунитет специфический, его составляющие научены ответу на точные молекулярные структуры. Для создания своих рецепторов адаптивный иммунитет использует перегруппировку генов (реаранжировку), и пролиферацию клеток со специфическими рецепторами путем формирования клонов. Адаптивный иммунитет имеет иммунологическую память. Адаптивная иммунная система — дополнение к эволюционно более древней врождённой иммунной системе, обеспечивающее специфичность распознавания и память.
Частью врожденного иммунитета являются барьеры организма. Они включают в себя эпителиальные слои, слизь для предотвращения прилипания микробов и антимикробные пептиды. Эти пептиды включают α — дефензины нейтрофилов, β — дефензины эпителиальных клеток и гистатины слюны.
В эффекторных механизмах иммунной системы (воспаление и реакция острой фазы) задействованы опсонизация, фагоцитоз, внутриклеточное уничтожение и секреция цитокинов. Бактерии имеют механизмами уклонения от эффекторных механизмов защиты, эффекторные механизмы иммунитета имеют ограниченное действие против вирусов.
Клеточное звено врожденного иммунитета представлено разными видами лейкоцитов: нейтрофилы составляют 50-70% лейкоцитов, лимфоциты 20-35%, моноциты 3-7%, эозинофилы 1-3% и базофилы 0-1%.
Нейтрофилы и макрофаги
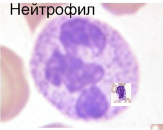
- Нейтрофилы и макрофаги являются наиболее важными фагоцитирующими клетками. Они образуются из полипотентных гемопоэтических стволовых клеток и дальнейшего дифференцирования миелоидного — предшественника (гранулоцито-моноцито колониеобразующей клетки).
Нейтрофилы и макрофаги обычно используют одни и те же механизмы уничтожения чужого, но нейтрофилы живут около суток, активируются при остром воспалении, и уничтожают только бактерии с использованием активных форм кислорода. Макрофаги, в отличие от нейтрофилов, живут недели, действуют при хроническом воспалении, атакуют многие микроорганизмы, презентируют антиген, секретируют множество цитокинов и используют оксид азота как реактивную форму кислорода.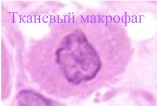
Работа нейтрофилов – фагоцитировать чужое. Нейтрофилы широко представлены циркуляции и тканях, и они очень мобильны и поэтому обычно первыми реагируют на возбудителя. В азурофильных гранулах нейтрофилы содержат гидролитические ферменты, дефензины и миелопероксидазу. Другие гранулы переносят рецепторы для комплемента, адгезии и цитокинов и готовы к экзоцитозу получив сигнал. Незрелые нейтрофилов еще не имеют характерного ядра полиморфноядерных клеток (зрелых нейтрофилов), ядро в виде палочки. Для распознавания и связывания мишеней нейтрофилы используют в основном Fc рецепторы и рецепторы комплемента, рецепторы распознавания образов.
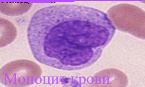 Макрофаги фагоцитируют патогены и презентируют антиген. Они могут что-то фагоцитировать, и освобождать антииммунные (толерогенные) сигналы, не секретировать сигналы, или секретировать проиммунные (иммуногенные) сигналы. В крови они
Макрофаги фагоцитируют патогены и презентируют антиген. Они могут что-то фагоцитировать, и освобождать антииммунные (толерогенные) сигналы, не секретировать сигналы, или секретировать проиммунные (иммуногенные) сигналы. В крови они
циркулируют как моноциты в течение суток, затем мигрируют в ткани, где дифференцируются в макрофаги (больше цитоплазмы, гранул и складчатая мембрана). Макрофаги имеют рецепторы к комплементу, Fc и рецепторы распознавания образов.- Макрофаги являются важнейшими регуляторами как адаптивного, так и врожденного иммунного ответ.
Естественны киллеры
- Естественны киллеры (ЕK) являются важными эффекторными лимфоцитами врожденного иммунитета, которые проявляют цитолитическую активность против различных аллогенных внутриклеточных мишеней в неспецифических, контакт-зависимых, не фагоцитарных процессах, которые не требует предварительной сенсибилизации антигеном. ЕК клетки имеют несколько свойств обычных цитотоксических Т-клеток (ЦЛТ), в том числе аналогичные механизмы цитолиза. Цитолитическая активность ЕК опосредована формированием пор в клетке-мишени с последующей секрецией в мишень белков, таких как гранзимы и перфорин, сериновые протеазы и другие. Их цитотоксическая активность позитивно регулируется с помощью IL-2, IL-15 и интерферонов, и негативно простагландинами и TGF-β.
- Естественные киллеры Т клетки (ЕКТ) – представляют собой различные линии Т-клеток, которые экспрессируют инвариантный Т-клеточный рецептор αβ (TCR αβ) и имеют на поверхности ряд маркеров, общих с ЕК. ЕКТ клетки рестриктированы по неполиморфной CD1d молекуле и активируются гликолипидами антигенов, представленными CD1d. Для идентификации мышиных и человеческих ЕKT может быть использованы CD160 и Vα24Jα18 соответственно
- Интраэпителиальные γδ Т-клетки (освобождают провоспалительные цитокины),
- B-1 клетки (синтез неспецифических «естественных» антитела).
Врожденный иммунитет активируется паттерн-распознающими рецепторами (PRRs), которые узнают паттерны патоген ассоциированных молекул (РАМРs, подобно ЛПС, CpG DNA, fMet, dsRNA и др.).
Паттерны патоген ассоциированных молекул должны быть экспрессированы на патогене, но отсутствовать у хозяина. Они имеют тенденцию к структурной инвариантности для группы возбудителей, и жизненно необходимы патогенам. Это полисахариды / нуклеотиды, но не белки.
Паттерн распознающие рецепторы (PRRs) являются генетически закодированной линией и не подвержены реаранжировке.
Взаимодействие паттерн распознающих рецепторов с патером патоген ассоциированных молекул инициирует внутриклеточные сигнальные каскады, которые обычно заканчиваются передачей сигнала в ядро и синтезом провоспалительных цитокинов.