Содержание:
Определение
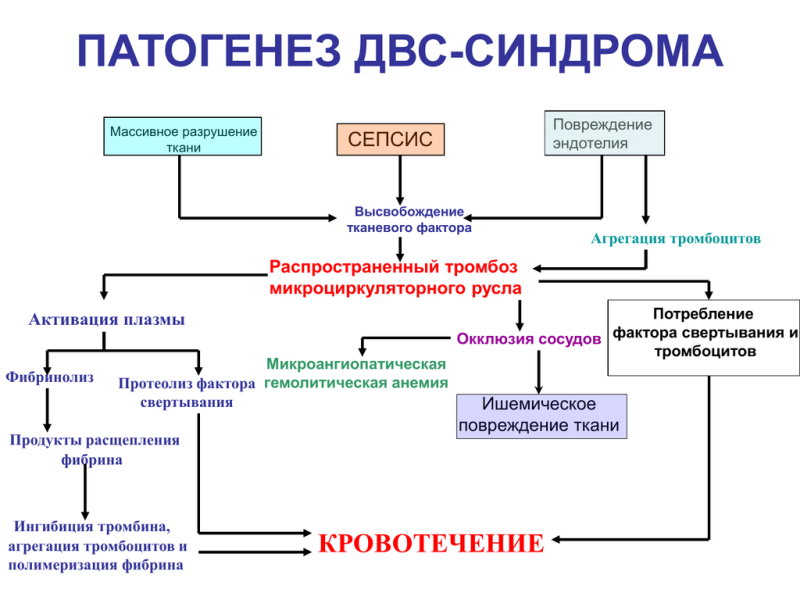
 ДВС (диссиминированное внутрисосудистое свертывание) — синдром, который характеризуется системной внутрисосудистой активацией свертывания крови, что приводит к широко распространенному отложению фибрина в циркуляции. Существуют хорошие экспериментальные и патологические доказательства того, что отложение фибрина способствует полиорганной недостаточности. Массовая и непрерывная активация свертывания может привести к истощению тромбоцитов и факторов свертывания крови, что проявляется кровотечениями (коагулопатия потребления). Следовательно, клиническая ситуация при ДВС характеризуется одновременными тромбозами и кровотечениями, которые могут представлять трудную проблему для клинициста.
ДВС (диссиминированное внутрисосудистое свертывание) — синдром, который характеризуется системной внутрисосудистой активацией свертывания крови, что приводит к широко распространенному отложению фибрина в циркуляции. Существуют хорошие экспериментальные и патологические доказательства того, что отложение фибрина способствует полиорганной недостаточности. Массовая и непрерывная активация свертывания может привести к истощению тромбоцитов и факторов свертывания крови, что проявляется кровотечениями (коагулопатия потребления). Следовательно, клиническая ситуация при ДВС характеризуется одновременными тромбозами и кровотечениями, которые могут представлять трудную проблему для клинициста.
Само по себе диссиминированное внутрисосудистое свертывание (ДВС) не болезнь, а осложнение различных заболеваний, наиболее тяжелыми из которых являются инфекции, воспаление, травмы и рак.
Клинические состояния, которые могут быть связаны с ДВС
- Сепсис / тяжелая инфекция (любой микроорганизм).
- Травма (например, политравма, нейротравма, жировая эмболия).
- Разрушение органа (например, и панкреатит).
- Малигнизация (злокачественные опухоли).
— опухоли,
— миелопролиферативные / лимфопролиферативные злокачественные новообразования. - Акушерские катастрофы- эмболия околоплодными водами- отслоение плаценты.
- Сосудистые нарушения- синдром Казабаха-Мерритт- аневризмы крупных сосудов.
- Тяжелая печеночная недостаточность.
- Тяжелые токсические или иммунологические реакции.
- Укусу змей.
- Наркотики.
- Реакции при переливании крови.
- Отторжение трансплантата.
С ДВС обычно связаны бактериальные инфекции, в частности, септицемии. Но системные инфекции вызванные вирусами и паразитами, так же могут привести к ДВС. Факторами, влияющие на развитие ДВС у пациентов с инфекциями, могут быть конкретные компоненты клеточной мембраны микроорганизма — липополисахарид или эндотоксин или бактериальные экзотоксины (например стафилококковый альфа -токсин). Эти компоненты могут привести к генерализованной воспалительной реакции, которая характеризуется повышенным уровнем цитокинов. Цитокины в основном продуцируется активированными мононуклеарами и эндотелиальными клетками и частично ответственны за срыв свертывающей системы в ДВС.
Тяжелая травма является еще одним клиническим состоянием часто связанным с ДВС. А сочетание поступления в кровоток материала тканей (жира, фосфолипиды) с гемолизом и повреждением эндотелия может способствовать системной активации свертывания крови. Кроме того, появляется все больше доказательств того, что цитокины, играют ключевую роль в развитии ДВС при травмах. На самом деле, спектр системных цитокинов практически идентичен у пациентов с травмами и сепсисом.
Как солидные опухоли, так и гемобластозы могут осложнить ДВС
Механизмы нарушения в системе свертывания в этой ситуации плохо понятны. Клетки солидных опухолей синтезируют прокоагулянтные молекулы, в том числе тканевый фактор и раковый прокоагулянт, активирующий фактор X в Ха. Раковый прокоагулянт обнаружен в экстрактах опухолевых клеток и в плазме пациентов с солидными опухолями. Особые формы ДВС синдрома часто встречается при остром промиелоцитарном лейкозе, который характеризуется выраженным фибринолитическим состоянием и активацией системы свертывания. Хотя клинически при промиелоцитарном лейкозе преобладают кровотечения, при аутопсии находят диссиминированный тромбоз.
Острый ДВС-синдром возникает при акушерских осложнениях таких как отслойка плаценты и эмболия околоплодными водами. Развитие ДВС при отслойке плаценты связывают с массированными поступлением в кровоток плацентарного тромбопластина — степень развития ДВС коррелирует со степенью отслоения плаценты. Амниотическая жидкость активирует свертывание крови.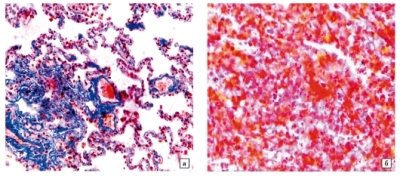
Хотя система свертывания крови может быть активирована у пациентов с преэклампсией и HELLP (гемолиз, повышение активности печеночных ферментов и низкие тромбоциты) синдромом, субклинические проявления и выраженный ДВС наблюдаются только у небольшого процента беременных.
Сосудистые заболевания, такие как крупные аневризмы аорты или гигантская гемангиома (синдром Казабаха-Мерритта), может привести к локальной активации свертывания, активированные факторы свертывания могут в конечном счете «переполнить» системный кровоток и быть причиной ДВС, но более распространенным при такой патологии является системное истощение факторов свертывания и тромбоцитов в результате локального потребления.
 Имеются убедительные данные подтверждающие мнение о том, что тканевой фактор является центральным медиатором активации коагуляции при сепсисе. Традиционно считалось, что ДВС — результат активации свертывания крови по внешнему и внутреннему пути. Исследования последних 15 лет показали, что образование тромбина при ДВС инициируется исключительно по внешнему пути (тканевый фактор/фактор VIIa). Тканевой фактор, способный связать VII и активировать его в VIIa, может быть экспрессирован на активированных и неактивированных мононуклеарных (моноциты и лимфоциты) и эндотелиальных клетках. VIIa затем активирует вниз по течению каскады свертывания.
Имеются убедительные данные подтверждающие мнение о том, что тканевой фактор является центральным медиатором активации коагуляции при сепсисе. Традиционно считалось, что ДВС — результат активации свертывания крови по внешнему и внутреннему пути. Исследования последних 15 лет показали, что образование тромбина при ДВС инициируется исключительно по внешнему пути (тканевый фактор/фактор VIIa). Тканевой фактор, способный связать VII и активировать его в VIIa, может быть экспрессирован на активированных и неактивированных мононуклеарных (моноциты и лимфоциты) и эндотелиальных клетках. VIIa затем активирует вниз по течению каскады свертывания.
Усиление отложения фибрина — недостаточность системы физиологических антикоагулянтов.
Физиологическая регуляция активности тромбина обычно осуществляется на трех уровнях свертывающей системы:
- на уровне тромбина и фактора Ха антитромбином;
- на уровне кофакторов V и VIII путем активированного протеина C;
- на уровне комплекса тканевый фактор / фактора VIIa ингибитором пути тканевого фактора (TFPI).
При ДВС, каждый из этих трёх основных физиологических антикоагулянтных механизмов поврежден.
 Антитромбин не в состоянии адекватно регулировать активность тромбина при ДВС по нескольким причинам:
Антитромбин не в состоянии адекватно регулировать активность тромбина при ДВС по нескольким причинам:
- Во-первых, антитромбин постоянно потребляется в условиях образования тромбина и активирования других протеаз, которые чувствительны к антитромбину;
- Во-вторых, комплекс антитромбин-тромбин гидролизует эластаза, освобождаемая активированными нейтрофилами;
- В третьих, нарушен синтез антитромбина из-за дисфункции печени при сепсисе и, наконец, происходит потеря этого ингибитора протеаз на уровне повышенной проницаемости капилляров.
Причины недостаточности системы протеина С при сепсисе и ДВС
- Во-первых, увеличивается потребление протеина С, которое протекает на фоне снижения синтеза белка в печени и потери сосудами.
- Во-вторых, активация сети цитокинов, в особенности высокий уровень фактора некроза опухолей (TNF-α), снижают экспрессию протеина С на эндотелии сосудов
- В третьих, ингибиторная способность протеина С снижена из-за низких уровней свободного протеина S, который образует комплекс с С4в компонентом комплемента. Плазменный уровень белков системы комплемента при сепсисе увеличивается в результате реакции острой фазы.
Экспериментально и клинически подтверждена недостаточность TFPI при развитии ДВС синдрома.
Важно понимать, что на сегодняшний день не существует единого лабораторного теста, который обладает достаточной чувствительностью или достаточно характерный для диагностики ДВС.
Система подсчета очков, которая использует простые лабораторные тесты. Подкомитетом по ДВС Международного общества по изучению тромбозов и гемостаза опубликован алгоритм диагностики ДВС на основе системы подсчета балов. Наличие основного заболевания, связанного с ДВС, является непременным условием для использования алгоритма. Ориентировочно, оценка ≥ 5 свидетельство в пользу ДВС.
Диагностика ДВС синдрома
- Оценка риска: имеет ли пациент основное заболевание, которое связано с развитием ДВС. Если да — используйте этот алгоритм, если нет – не используйте.
- Выполнить общекоагуляционные тесты (количество тромбоцитов, протромбиновое время [ПТВ], фибриноген, растворимые мономеры фибрина или продукты распада фибрина).
- Оценка результатов исследования коагуляции:
• количество тромбоцитов (> 100 = 0,