Содержание:
Здесь мы описываем природу и функцию тканевых макрофагов в разных органах
Легкое
 Люди дышат воздухом для газообмена, но через дыхание в организм могут проникать бактерии, вирусы, грибы, органические и неорганические вещества.
Люди дышат воздухом для газообмена, но через дыхание в организм могут проникать бактерии, вирусы, грибы, органические и неорганические вещества.
Мф и нейтрофилы уничтотают бактерии, используя механизмы врожденного иммунитета легкого. Установлено, что Мф, мигрировавшие в легкие из желточного мешка плода, находятся в периферической интерстициальной ткани легких, Мф, пришедшие из печени плода, локализуются в альвеолах, а Мф костного мозга находится в центральной интерстициальной ткани. Альвеолярные Мф на поверхности клетки содержат C-лектин рецепторную группу (рецептор маннозы, рецептор глюкана β-D, фагоцитарный рецептор и рецептор комплемента), которая распознает внедрившихся патогенов. Распознавание туберкулеза осуществляют TLR2, объединенный с TLR1 или TLR6. Однако некоторые виды туберкулеза устойчивы к киллингу в фагосомах макрофагов. В этом случае Мф и лимфоциты ограничивают туберкулез путем образования гранулемы. В легочной ткани комплемент, сурфактатные гидрофильные протеиды SP-A, SP-D, IgA, лизоцим, интерфероны, лактоферрины, дефенсины, растворимый CD14, хемокины и цитокины работают вместе, образуя гуморальную иммунную систему органа.
Образование и созревание альвеолярных макрофагов индуцируется рецепторами, активируемыми пероксисомными пролифераторами-гамма — ядерными рецепторами (PPAR-γ). Контроль активация PPAR-γ в альвеолярных макрофагах легких осуществляется гранулоцитарно-макрофагальным колониестимулирующим фактором(GM-CSF). PPAR-γ не только действует как фактор транскрипции в метаболизме липидов и углеводов, но также играет важную роль в воспалении, восстановлении тканей, деградации сурфактанта, фагоцитозе и выживаемости клеток. PPAR-γ также индуцирует экспрессию на фагоцитах рецептора CD36 — фагоцитоз липидов и апоптотических нейтрофилов. Кроме того, для дифференциации и гомеостаза алвеолярных макрофагов необходим трансформирующий фактор роста (TGF)-β. TGF-β контролирует альвеолярные Мф по аутокринному механизму. TGF-β также регулирует экспрессию генов, связанных с дифференциацией альвеолярных макрофагов и их метаболизмом.
Фагоцитарная способность альвеолярных макрофагов ухудшается несколькими патологическими состояниями. Например, хроническое употребление алкоголя вызывает дисфункцию альвеолярных макрофагов. Алкоголь подавляет экспрессию рецепторов GM-CSF на клеточной поверхности альвеолярных макрофагов и ухудшает их иммунную функцию.
При ВИЧ-инфекции альвеолярные Мф инфицированы ВИЧ, а у инфицированных клеток нарушена фагоцитарная функция, окислительный взрыв и секреция цитокинов.
Печень
 Через воротную вену печень всегда подвергается воздействию антигенов из желудочно-кишечного тракта, включая пищевые антигены и бактериальные компоненты. Кишечные бактерии (более 1 × 1012 клеток) обычно проживают в желудочно-кишечном тракте, а гомеостаз в организме поддерживается через иммунорегуляторные механизмы, которые подавляют иммунный ответ на чужеродные антигены или бактериальные антигены в кишечнике. Клетки Купфера являются самоподдерживающейся популяцией макрофагов в печени, полученны из моноцитов печени плода, и отличаются от макрофагов, образующихся из моноцитов, которые быстро накапливаются в поврежденной печени.
Через воротную вену печень всегда подвергается воздействию антигенов из желудочно-кишечного тракта, включая пищевые антигены и бактериальные компоненты. Кишечные бактерии (более 1 × 1012 клеток) обычно проживают в желудочно-кишечном тракте, а гомеостаз в организме поддерживается через иммунорегуляторные механизмы, которые подавляют иммунный ответ на чужеродные антигены или бактериальные антигены в кишечнике. Клетки Купфера являются самоподдерживающейся популяцией макрофагов в печени, полученны из моноцитов печени плода, и отличаются от макрофагов, образующихся из моноцитов, которые быстро накапливаются в поврежденной печени.
Клетки Купфера поселяются вместе с синусоидальными эндотелиальными клетками и являются важными фагоцитами, которые постоянно очищают кровь от дериватов бактерий кишечника. Клетки Купфера поддерживают гомеостаз функционального железа и метаболизм билирубина. На поверхности клеток Купфера есть Fc-рецепторы и различные рецепторы-фагоцитоза, озволяющие им удалять поврежденные эритроциты, гемоглобин-гаптоглобиновые комплексы и содержащие дереваты гемоглобина эритроцитов везикулы из крови. Они также контролируют метаболизм холестерина путем синтеза белка переносчика эфиров холестерина, что важно для переноса холестерина из липопротеинов высокой плотности (ЛПВП) в липопротеины очень низкой плотности.
При повреждениях печени клетки Купфера выделяют противовоспалительные цитокины, такие как IL-10, IL-4, и IL-13. Интересно, что как резидентные, так и Мф, полученные моноцитов крови, взаимодействуют при восстановлении тканей. Их полезные действия включают ослабление нейтрофильного воспаления через синтез простагландина (PGE)-2, фагоцитоз мертвых клеток и восстановление структур сосудов с использованием факторов ангиогенеза, таких как фактор роста эндотелия сосудов (VEGF)-A.
Как альвеолярные Мф, так и клетки Купфера происходят из моноцитов печени плода, но их реакция на окружающие раздражители совершенно различна, что говорит о влиянии окружающей среды на дифференциацию тканевых макрофагов.
Кроме того, активированные клетки Купфера являются основным источником макрофагального воспалительного белка-2 (MIP-2) при повреждениях печени. MIP-2 играет двойную роль в опосредовании воспаления печени и стимулировании регенерации печени.
Головной мозг
 Микроглия (Мф мозга) происходит из эритромиелоидных предшественников желточного мешка во время примитивного гемопоэза раннего эмбрионального развития и поддерживаются примерно на 100% от их начальной концентрации в течение жизни. Микроглия, тип глиальных клеток, быстро реагирующих на повреждения головного мозга, нейродегенеративные заболевания, церебральную ишемию, и активируются для выполнения различных функций. Микроглия экспрессирует различные рецепторы; LPS, пептидные гликаны или вирусные гликопротеины, связанные TLR, активируют микроглию.
Микроглия (Мф мозга) происходит из эритромиелоидных предшественников желточного мешка во время примитивного гемопоэза раннего эмбрионального развития и поддерживаются примерно на 100% от их начальной концентрации в течение жизни. Микроглия, тип глиальных клеток, быстро реагирующих на повреждения головного мозга, нейродегенеративные заболевания, церебральную ишемию, и активируются для выполнения различных функций. Микроглия экспрессирует различные рецепторы; LPS, пептидные гликаны или вирусные гликопротеины, связанные TLR, активируют микроглию.
Кроме того, микроглию активируют конечные продукты гликирования, белок амилоида-бета, различные агрегированные белки, поврежденные ткани мозга. Активированная микроглия производит как несколько факторов, связанных с нейропротекцией — противовоспалительные цитокины и нейротропные факторы), но также и факторы повреждения нервов (воспалительные цитокины, оксид азота (NO), ROS, возбуждающие аминокислоты и АТФ). При болезни Альцгеймера активация микроглии амилоидом-β сопровождается секрецией факторов повреждения нервов. Прямое влияние на нейропротекцию оказывают IL-6, IL-2, IL-3,GM-CSF и эритропоэтин, тогда как цитокины, такие как IL-1,IL-4, IL-5 и TGF-β оказывают косвенный эффект нейропротекции, индуцируя секрецию фактор роста нервов (NGF) в астроцитах.
При повреждении нейронов микроглия активируется и мигрирует к местку травмы. Эта миграция индуцируется АТФ или АДФ, высвобождаемыми из поврежденных клеток. Активированная микроглия имеет амебоидную форму.
Амебоидная микроглия может фагоцитировать мертвые клетки и инородные материалы. Считается, что это явление способствует поддержанию здоровья мозга и предотвращает освобождение неблагоприятных факторов.
Кишечник
 Как упоминалось ранее, Мф в кишечном тракте после рождения замежаются макрофагами, образующимися из моноцитов костного мозга. Мф кишечника действуют как врожденные иммунные клетки через фагоцитоз и уничтожение чужеродных веществ, таких как бактерии, и играют центральную роль в защите хозяина от инфекции. Кишечные Мф не имеют ToLL рецепторов, распознающих бактерии, что определяет их невосприимчивость к бактериальным антигенам. Кроме того, оседлые кишечные Мф продуцируют IL-10 и непосредственно участвуют в иммуносупрессии.
Как упоминалось ранее, Мф в кишечном тракте после рождения замежаются макрофагами, образующимися из моноцитов костного мозга. Мф кишечника действуют как врожденные иммунные клетки через фагоцитоз и уничтожение чужеродных веществ, таких как бактерии, и играют центральную роль в защите хозяина от инфекции. Кишечные Мф не имеют ToLL рецепторов, распознающих бактерии, что определяет их невосприимчивость к бактериальным антигенам. Кроме того, оседлые кишечные Мф продуцируют IL-10 и непосредственно участвуют в иммуносупрессии.
Через IL-10 кишечные Мф контролируют поддержание дифференциации, пролиферации и функции периферических регуляторных Т-клеток (pTregs). Кишечные Мф и pTregs являются первичными IL-10-продуцирующие клетки в слизистой оболочке кишечника. Поэтому эти сети иммунных клеток важны для иммунной толерантности к привычным антигенам в слизистой оболочке кишечника.
Кроме того, в ответ на повреждение слизистой оболочки кишечника IL-10 макрофагов индуцирует синтез сигнального белка 1 (WISP-1). WISP-1 индуцирует пролиферацию эпителиальных клеток и восстановление ран путем активации эпителиальных пропролиферативных путей. В индукции толерантности кишечника принимают участие и Мф CD169+ , которые распределяются почти по всей области собственной пластинки. После травмы слизистой оболочки CD169 + Мф продуцируют CCL8 — хемокин, который рекрутирует из крови моноциты воспаления.
Селезенка
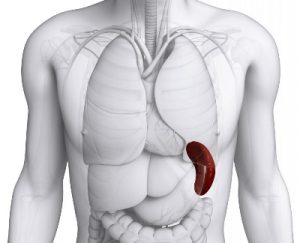 Селезенка является органом с несколькими различными видами макрофагов, полученных из моноцит фетальной печени. Селезенка содержит отдельные анатомические области красной и белой пульпы, разделенных краевой зоной. Тканевые Мф в селезенке:
Селезенка является органом с несколькими различными видами макрофагов, полученных из моноцит фетальной печени. Селезенка содержит отдельные анатомические области красной и белой пульпы, разделенных краевой зоной. Тканевые Мф в селезенке:
- Мф красной пульпы,
- металлофильные Мф маргинальной зоны, распределенные внутри маргинальной зоны,
- Мф маргинальной зоны, распределенные вне маргинальной зоны,
- Мф, распределенные в лимфатическом фолликуле белой пульпы
Макрофаги красной пульпы улавливают поврежденные клетки крови, перерабатывают железо и катаболизируют гем, фагоцитируют возбудителей инфекций, передваемых через кровь (Plasmodium, Cryptococcus neoformans, Streptococcus pneumoniae, Salmonella typhimurium).
Металлофильные макрофаги: непосредственно активируют Т киллеры (T клетки CD8+), фагоцитируют передаваемые через кровь инфекции (Listeria monocytogenes, LCMV)
Макрофаги маргинальной зоны:
- Поглощение модифицированного липопротеидов низкой плотности
- Т хелперы 2 зависимая активация В клеток
- Фагоцитоз передаваемых через кровь патогенов (Staphylococcus aureus, Listeria monocytogenes, Escherichia coli, HIV, LCMV)
- Оба вида маргинальных макрофагов играют важную роль в обучении иммунной толерантности при фагоцитозе мертвых клеток.
Макрофаги белой пульпы. Зародышевой центр белой пульпы селезенки — это место, где B лимфоциты созревают и дифференцируются. Клетки, экспрессирующие B-клеточные рецепторы с высокой аффинностью к антигенам, выживают, а те, у кого рецепторы с низким сродством подвергаются апоптозу.
Жировая ткань
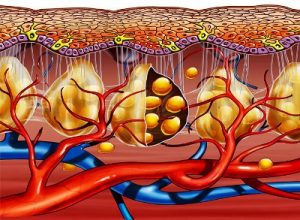 У пациентов с ожирением между увеличенными жировыми клетками выявляются инфильтраты макрофагов и эти Мф происходят из моноцитов костного мозга. Почти все Мф инфильтратов являются макрофагами M1, которые секретируют воспалительные цитокины, такие как фактор некроза опухоли (TNF) -α и IL-6, что усугубляет воспаление. Воспалительные цитокины, продуцируемые макрофагами M1, действуют на окружающие жировые клетки и ослабляют их чувствительность к инсулину. В результате жировые клетки обладают сниженной способностью к поглощению глюкозы, увеличивая риск диабета. Мф в жировой ткани здоровых людей представлены подтипом M2. M2 Мф в жировой ткани участвуют в поддержании нормального уровня сахара в крови через секрецию инсулиноподобного фактора роста (IGF) -1.Свободные жирные кислоты, которые находятся в более высоких концентрациях у пациентов с ожирением, действуют на Мф и контролируют воспалительную реакцию. Пальмитиновая кислота, насыщенная жирная кислота, связывается с TLR2 или TLR4 на макрофагах и индуцирует воспалительный ответ. Кроме того, MCP-1 (CCL2), член семейства хемокинов, активируется в увеличенных жировых клетках и вызывает миграцию и инфильтрацию макрофагов в жировой ткани.
У пациентов с ожирением между увеличенными жировыми клетками выявляются инфильтраты макрофагов и эти Мф происходят из моноцитов костного мозга. Почти все Мф инфильтратов являются макрофагами M1, которые секретируют воспалительные цитокины, такие как фактор некроза опухоли (TNF) -α и IL-6, что усугубляет воспаление. Воспалительные цитокины, продуцируемые макрофагами M1, действуют на окружающие жировые клетки и ослабляют их чувствительность к инсулину. В результате жировые клетки обладают сниженной способностью к поглощению глюкозы, увеличивая риск диабета. Мф в жировой ткани здоровых людей представлены подтипом M2. M2 Мф в жировой ткани участвуют в поддержании нормального уровня сахара в крови через секрецию инсулиноподобного фактора роста (IGF) -1.Свободные жирные кислоты, которые находятся в более высоких концентрациях у пациентов с ожирением, действуют на Мф и контролируют воспалительную реакцию. Пальмитиновая кислота, насыщенная жирная кислота, связывается с TLR2 или TLR4 на макрофагах и индуцирует воспалительный ответ. Кроме того, MCP-1 (CCL2), член семейства хемокинов, активируется в увеличенных жировых клетках и вызывает миграцию и инфильтрацию макрофагов в жировой ткани.
Сердце
 Подавляющее большинство резидентных сердечных макрофагов происходит из эмбрионального желточного мешка и предшественников печени плода. Пополнение происходит со скоростью примерно один раз в месяц посредством пролиферации. При этом субпопуляция макрофагов CCR2+ пополняется рекрутированием моноцитов крови и локальной пролиферацией, тогда как CCR2— Мф репопулируются в основном локальной пролиферацией. С возрастом самообновление резидентных сердечных макрофагов снижается, а моноциты крови все чаще вносят вклад в популяцию макрофагов сердца.
Подавляющее большинство резидентных сердечных макрофагов происходит из эмбрионального желточного мешка и предшественников печени плода. Пополнение происходит со скоростью примерно один раз в месяц посредством пролиферации. При этом субпопуляция макрофагов CCR2+ пополняется рекрутированием моноцитов крови и локальной пролиферацией, тогда как CCR2— Мф репопулируются в основном локальной пролиферацией. С возрастом самообновление резидентных сердечных макрофагов снижается, а моноциты крови все чаще вносят вклад в популяцию макрофагов сердца.
Доказано, что макрофаги сердца
- Модулируют сердечную электрическую проводящую систему.
- Определяют исход инфаркт миокарда.
- С изменениями фенотипа и числа макрофагов связаны сердечная недостаточность и диабет или воспалительные заболевания сердца, такие как саркоидоз и миокардит, что, в свою очередь, может способствовать развитию аритмий и нарушению проводимости.
Опухоли
Имеются убедительные клинические и экспериментальные данные о том, что макрофаги способствуют развитию рака и развитию злокачественных новообразований. Во время инициирования опухоли они создают воспалительную среду, которая мутагенна и способствует росту. По мере развития опухолей до злокачественности макрофаги стимулируют ангиогенез, усиливают миграцию и инвазию опухолевых клеток и подавляют противоопухолевый иммунитет. На метастатических участках макрофаги готовят ткань-мишень для поступления опухолевых клеток, а затем другая субпопуляция макрофагов способствует экстравазации опухоли, выживанию и последующему росту. Специализированные субпопуляции макрофагов могут представлять собой важные новые терапевтические цели.